Nung nóng 22,4 gam Cr(OH)3 ở điều kiện phòng (nhiệt độ= 20;P=1 atm). Tính lượng nước thu được, biết H%=90% và ở điều kiện (nhiệt độ=20 độ, p=1 atm) ,thể tích 1 mol khí là 24,5 lít.
[hóa học 8]
Một bình cầu dung tích 20 lít chứa ôxi ở nhiệt độ 16 ° C và áp suất 100 atm. Tính thể tích của lượng khí này ở điều kiện chuẩn. Tại sao kết quả tìm được chỉ là gần đúng
V 0 ≈ 1,889 lít. Vì áp suất quá lớn nên khí không thể coi là khí lí tưởng. Do đó kết quả tìm được chỉ là gần đúng.
nung 15,6g nham ( Al(OH)3 thu được bao nhiêu gam oxit và bao nhiêu lít hơi nước ở điều kiện phòng(pit rằng ở điều kiện phòng nhiệt độ=20 độ c, p=1atm-->24l
Al(OH)3----> Al2O3+H2O
nAl(OH)3 = \(\frac{m}{M}\) =\(\frac{15,6}{78}\) = 0.2(mol)
PTPƯ: 2Al(OH)3 -> Al2O3 + 3H2O
0,4 0,2 0,2
mAl2O3 = n. M= 0,2 . 102 = 20,4 (g)
nH2O = \(\frac{P.V}{R.T}\) -> P.V = nRT
-> 1 . V= nRT -> V = nRT
<-> 0,2 . 0,082 . ( 273 + 20) = 24,4772 ( lít)
Trong phòng thí nghiệm người ta điều chế được 0,4 lít khí H2 ở điều kiện tiêu chuẩn ![]() .
.
Hỏi thể tích của lượng khí trên ở áp suất 0,5 atm và nhiệt độ 170C bằng bao nhiêu?
A. 0,77 lít
B. 0,83 lít
C. 0,5 lít
D. 1,27 lít
Đáp án A
Gọi ![]() lần lượt là áp suất, thể tích và nhiệt độ của khối khí ở trạng thái ban đầu
lần lượt là áp suất, thể tích và nhiệt độ của khối khí ở trạng thái ban đầu
![]()
![]()
Gọi ![]() lần lượt là áp suất, thể tích và nhiệt độ của khối khí ở trạng thái sau:
lần lượt là áp suất, thể tích và nhiệt độ của khối khí ở trạng thái sau:
![]()
Áp dụng phương trình trạng thái của khí lí tưởng ta có:
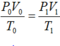
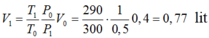
Điều kiện tiêu chuẩn : nhiệt độ .......... , áp suất ............ -
Thể tích mol phân tử của chất khí là thể tích chứa .......... phân tử khí hay ......... mol chất khí. -
Ở đktc , thể tích của 1 mol chất khí bằng ......... lít.
- Người ta quy ước điều kiện thường là ở nht độ .......... và áp suất ......... atm.
Điều kiện tiêu chuẩn : nhiệt độ 0oC , áp suất 1 atm.
Thể tích mol phân tử của chất khí là thể tích chứa 6,022.1023 phân tử khí hay 1 mol chất khí.
Ở đktc , thể tích của 1 mol chất khí bằng 22,4 lít.
Người ta quy ước điều kiện thường là ở nht độ 20oC và áp suất 1 atm.
Điều kiện tiêu chuẩn : nhiệt độ 0oC , áp suất 1 atm
Thể tích mol phân tử của chất khí là thể tích chứa 6.1023 phân tử khí hay 1 mol chất khí. -
Ở đktc , thể tích của 1 mol chất khí bằng 22,4 lít.
- Người ta quy ước điều kiện thường là ở nht độ 20oC và áp suất 1 atm.
Điều kiện tiêu chuẩn : nhiệt độ ....0oC...... , áp suất ..1atm.......... -
Thể tích mol phân tử của chất khí là thể tích chứa ....6 * 1023...... phân tử khí hay ....1..... mol chất khí. -
Ở đktc , thể tích của 1 mol chất khí bằng ...22,4...... lít.
- Người ta quy ước điều kiện thường là ở nhiệt độ ....20oC...... và áp suất ....1..... atm.
Một khí cầu có thể tích V = 336 m 3 và khối lượng vỏ m = 84 kg được bơm không khí nóng tới áp suất bằng áp suất không khí bên ngoài. Không khí nóng phải có nhiệt độ bằng bao nhiêu để khí cầu bắt đầu bay lên ? Biết không khí bên ngoài có nhiệt độ 27 ° C và áp suất 1 atm ; khối lượng mol của không khí ở điều kiện chuẩn là 29. 10 3 kg/mol.
Gọi ρ 1 và ρ 2 là khối lượng riêng của không khí ở nhiệt độ T 1 = 27 + 273 = 300 K và nhiệt độ T 2 là nhiệt độ khi khí cầu bắt đầu bay lên.
Khi khí cầu bay lên:
F Á c - s i - m é t = P v ỏ k h í c ầ u + P c ủ a k h ô n g k h í n ó n g
ρ 1 gV = mg + ρ 2 gV
ρ 2 = ρ 1 – m/V (1)
Ở điều kiện chuẩn, khối lượng riêng của không khí là:
ρ 0 = 29g/22,4l = 1,295g/ d m 3 = 1,295kg/ m 3
Vì thể tích của một lượng khí tỉ lệ thuận với nhiệt độ tuyệt đối khi áp suất không đổi nên khối lượng riêng của một lượng khí tỉ lệ nghịch với nhiệt độ tuyệt đối khi áp suất không đổi.
Ta có: ρ 1 = T 0 ρ 0 / T 1 (2)
Từ (1) và (2) suy ra: ρ 1 = 1,178 kg/ m 3
Do đó ρ 2 = 0,928 kg/ m 3
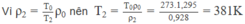
t 2 = 108 ° C
Người ta điều chế khí hiđrô và chứa vào một bình lớn dưới áp suất 1 atm, ở nhiệt độ 20 ° C. Tính thể tích khí phải lấy từ bình lớn ra để nạp vào một bình nhỏ thể tích 20 lít dưới áp suất 25 atm. Coi nhiệt độ không đổi.
Để điều chế khí oxi trong phòng thí nghiệm, người ta tiến hành phân hủy 24,5 gam kaliclorat KClO3 ở nhiệt độ cao.
a) Tính thể tích khí oxi thu được ở điều kiện tiêu chuẩn.
b) Lượng khí oxi thu được được dùng để oxi hóa hoàn toàn một lượng phôt pho đỏ (P) vừa đủ.
Viết PTHH của phản ứng trên và tính khối lượng sản phẩm P2O5 thu được.
c)Nếu dùng không khí để oxi hóa lượng P dùng ở phần (b) thì cần lấy bao nhiêu lít không khí? Biết rằng khí oxi chiếm ~ 20% thể tích không khí.
2KClO3-to>2KCl+3O2
0,2---------------------0,3
4P+5O2-to->2P2O5
--0,3-------0,12 mol
n KClO3=\(\dfrac{24,5}{122,5}=0,2mol\)
=>VO2=0,3.22,4=6,72l
=>m P2O5=0,12.142=17,04g
=>Vkk=6.72.5=33,6l
nKClO3 = 24,5 : 122,5 = 0,2 (mol)
pthh : 2KClO3 -t--> 2KCl +3 O2
0,2---------------------> 0,3(MOL)
VO2 = 0,3 .22,4 = 6,72 (L)
pthh : 4P+5O2-t--> 2P2O 5
0,3---> 0,12 (mol)
=> mP2O5 = 0,12 . 142 = 17,04 (g)
ta co : Vkk = VO2:21% = 6,72 : 21% 32 (l)
Trong một bình kín dung tích 20 lít có chứa 4,4 kg khí cacbonic ở nhiệt độ 27 ° C. Tính áp suất của khí trong bình. Biết thể tích của một mol khí ở điều kiện chuẩn là V 0 = 22,4 lít.
Gọi n là số mol khí cacbonic chứa trong bình: n = m/ μ , trong đó M là khối lượng khí cacbonic có trong bình, μ là khối lượng mol của khí cacbonic.
Ta có n = 100 mol
Nếu gọi V 0 là thể tích của lượng khí cacbonic ở điều kiện chuẩn ( p 0 = 1,013. 10 5 Pa; T 0 = 273 K) thì V 0 = n v 0
Áp dụng phương trình trạng thái của khí lí tưởng cho lượng khí cacbonic:
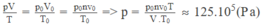
Câu 14: Nhiệt độ và áp suất ở điều kiện tiêu chuẩn của chất khí là
A. 00C, 20 atm. B. 00C, 1 atm.
C. 10C, 0 atm. D. 200C, 1 atm.